Perché il monitoraggio basato sul rischio è in aumento?
Monitoraggio basato sul rischio negli studi clinici
Cos'è il monitoraggio basato sul rischio?
Il monitoraggio basato sul rischio è il processo finalizzato a garantire la qualità degli studi clinici attraverso l'individuazione, la valutazione, il monitoraggio e la mitigazione dei rischi che potrebbero comprometterne la qualità o la sicurezza. Secondo le linee guida della Food and Drug Administration (FDA) statunitense, un approccio al monitoraggio basato sul rischio si articola in tre fasi:
- Individuare dati e processi critici. Al fine di monitorare in modo accurato la qualità di uno studio e la sicurezza dei suoi partecipanti, lo sponsor deve sapere quali sono gli elementi più importanti per ogni studio specifico, a partire dal consenso informato fino allo screening dell'idoneità e al monitoraggio degli eventi avversi.
- Effettuare una valutazione dei rischi. Ciò comporta l'identificazione delle fonti di rischio specifiche e delle conseguenze prodotte da eventuali errori di studio riconducibili a tali rischi.
- Sviluppare un piano di monitoraggio. Secondo le linee guida della FDA, il piano di monitoraggio dovrebbe "descrivere i metodi, le responsabilità e i requisiti di monitoraggio dello studio". Il suo obiettivo, infatti, è rendere noti i rischi e le procedure di monitoraggio a tutte le figure coinvolte nelle attività di monitoraggio dello studio.
Perché il monitoraggio basato sul rischio è in aumento?
Il costo e la complessità degli studi clinici sono aumentati notevolmente negli ultimi anni. Fino a un terzo del costo di uno studio ora è attribuibile alle tradizionali attività di analisi in loco dei dati clinici.
Questo approccio, fortemente legato alla verifica completa dei dati di origine, oltre ad essere dispendioso in termini di risorse, ha dimostrato una limitata capacità di identificazione e prevenzione dei problemi.
Dal momento che l'efficienza del monitoraggio è di fondamentale importanza per proteggere il benessere dei partecipanti agli studi e garantire l'integrità dei risultati finali, l'esigenza di aggiornare il processo di monitoraggio degli studi clinici è ampiamente condivisa.
Secondo quanto riportato da diversi enti di controllo, inclusa la FDA, il metodo utilizzato in via preferenziale per il monitoraggio degli studi clinici oggi è costituito da un approccio più centralizzato basato sul rischio.
Perché è migliore?
Una caratteristica fondamentale del monitoraggio basato sul rischio è l'utilizzo di tecniche di monitoraggio centralizzato. A differenza del monitoraggio in loco, basato sulla verifica completa dei dati di origine, il monitoraggio centralizzato garantisce una serie di vantaggi:
- Meno errori. I metodi di monitoraggio in loco, come qualsiasi operazione manuale, hanno una portata limitata e sono soggetti a errori. Il monitoraggio centralizzato basato sul rischio utilizza analisi più automatizzate per valutare la necessità di intervento manuale e offre maggiori probabilità di rilevare eventuali errori.
- Costi inferiori. Grazie al monitoraggio centralizzato, attività come gli audit in loco possono essere limitate ai siti degli studi in cui è più probabile che si verifichino problemi. In questo modo, è possibile ridurre notevolmente i costi di monitoraggio.
- Analisi migliori. Dal momento che tutti i dati confluiscono in un dashboard dei rischi centrale, i controlli grafici e statistici possono essere utilizzati molto più facilmente per stabilire l'eventuale presenza di outlier o pattern insoliti nei dati.
- Confronto tra più siti. Il monitoraggio centralizzato consente anche di confrontare i dati tra siti diversi per valutare le prestazioni, identificare dati potenzialmente fraudolenti o localizzare apparecchiature difettose o tarate in modo errato.
- Risultati più tempestivi. L’uso di un apposito dashboard consente inoltre di identificare e risolvere eventuali problemi mentre lo studio è in corso.
Il processo di monitoraggio
Come affermato in precedenza, la FDA ha fornito linee guida dettagliate per l'elaborazione di un piano di monitoraggio. Tuttavia, una volta attivato il piano, il compito di applicarlo spetta allo sponsor (o al suo delegato, ad esempio un'organizzazione di ricerca a contratto). Anche se le specifiche varieranno fortemente tra i diversi studi, un programma di monitoraggio orientato al rischio in genere comprenderà le attività riportate di seguito, che passeranno tutte attraverso un dashboard dei rischi completo realizzato ad hoc per un determinato studio:
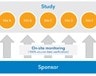
- Raccolta e invio di dati. Un approccio centralizzato richiede un flusso stabile e affidabile di dati da ciascun sito aderente allo studio verso il sistema di monitoraggio centrale. Questo può avvenire con operazioni manuali di inserimento e trasferimento dei dati pertinenti o attraverso un collegamento automatizzato tra il sistema di inserimento dati e il dashboard centrale.
- Monitoraggio tramite dashboard. La funzione del dashboard è fornire una vista immediata delle informazioni sullo stato di ciascun sito aderente allo studio in relazione ai fattori di rischio specifici nel trial in oggetto. Se un sito presenta un livello di rischio elevato, il piano di monitoraggio dovrebbe consentire di decidere se sia opportuno effettuare ulteriori indagini, da un'analisi statistica approfondita alla verifica dei dati in loco.
- Analisi statistica. Oltre a monitorare il dashboard dei rischi, può essere utile eseguire analisi statistiche supplementari per identificare i problemi. Semplici istogrammi e box plot possono rivelarsi estremamente utili per rilevare eventuali outlier tra siti e paesi diversi in relazione a vari indicatori di rischio. Tecniche più avanzate quali la clusterizzazione possono inoltre aiutare a individuare siti problematici e persino casi di frode.
- Indagini mirate in loco. Il monitoraggio tramite dashboard e le ulteriori analisi a volte possono segnalare la chiara necessità di effettuare indagini di persona in un determinato sito. In questi casi, potrebbe essere opportuno recarsi sul posto per condurre attività più tradizionali di verifica dei dati di origine, a seconda della natura dello studio. Il punto è che, una volta attivato un sistema centralizzato, le indagini in loco dovrebbero rappresentare l'eccezione, non la regola.
Il dashboard dei rischi
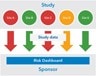
Il dashboard dei rischi costituisce il fulcro del programma di monitoraggio basato sul rischio. Tutti i dati dello studio dovrebbero confluire all'interno del dashboard, che deve essere progettato in modo tale da fornire indicazioni visive esplicite per i siti ad alto rischio.
Per consentire la creazione di queste indicazioni visive, nel piano di monitoraggio vengono spesso definite soglie corrispondenti a un livello di rischio lieve, moderato o forte da applicare a determinati indicatori di rischio. Utilizzando tali soglie, sarà possibile impostare il dashboard con un sistema a colori per riepilogare i livelli di rischio in base al sito o persino a seconda del paese.
Oltre alla funzione di base del dashboard dei rischi, dovrebbe anche essere possibile personalizzare la visualizzazione dei dati ed effettuare rapidamente ulteriori analisi. Gli analisti dovrebbero essere liberi di definire set multipli di soglie di rischio per valutare la sensibilità dei risultati ottenuti. Inoltre, dovrebbero essere in grado di calcolare metriche sui rischi complessivi per valutare le prestazioni globali di un determinato sito o paese.
Come iniziare: affrontare il cambio organizzativo
Sebbene l'approccio basato sul rischio sia al centro di un acceso dibattito nel settore e registri un crescente consenso in virtù dei vantaggi che offre, l'adozione di queste tecniche procede a rilento. Senza dubbio, il passaggio a un sistema di monitoraggio più centralizzato comporta sforzi notevoli e pone una serie di interrogativi: avete le competenze analitiche per monitorare i dati a livello centrale? Avete gli strumenti necessari per creare un dashboard utile? Che metodo utilizzate per raccogliere e trasmettere i dati dai siti in cui si svolgono i test? Cosa farà il personale attualmente impiegato nelle revisioni in loco?
In definitiva, il passaggio al monitoraggio basato sul rischio potrebbe essere più facile di quanto pensiate, anche perché alcuni strumenti sono sorprendentemente accessibili. Ecco alcuni passaggi per iniziare con il piede giusto:
- Trovate un promotore e uno sponsor esecutivo.
Un importante cambiamento organizzativo non può avvenire senza un promotore interno e uno sponsor esecutivo. In alcuni casi, entrambi i ruoli potrebbero essere ricoperti dalla stessa persona, ma in genere il promotore è un professionista che vede l'esigenza di cambiamento, ne comprende il potenziale e vende l'idea a uno sponsor esecutivo che si occuperà quindi di spianare la strada al cambiamento. - Acquisite gli strumenti giusti.
Il monitoraggio centralizzato potrebbe richiedere una serie di tecnologie, ma è meglio partire con strumenti che offrono rapidamente risultati visivi, senza bisogno di database di grandi dimensioni, operazioni di programmazione o persino conoscenze di statistica. Queste competenze potrebbero essere utili a lungo andare, ma non dovrebbero essere necessarie nella fase iniziale. - Partite in piccolo.
Dopo aver progettato un processo di monitoraggio di base e aver acquisito gli strumenti necessari, provate ad avviare le operazioni di valutazione dei rischi e monitoraggio centralizzato su un unico studio o un piccolo gruppo di studi. In questo modo, la vostra organizzazione dovrà ricorrere a una quantità limitata di risorse e potrà affrontare il cambiamento in modo graduale. - Adattate il processo in modo organico.
Partire in piccolo vi offre anche la possibilità di decifrare gli intoppi nel processo di monitoraggio, che, diventando più efficiente a ogni iterazione, potrà essere adattato più facilmente a un numero sempre maggiore di studi. Un approccio di questo genere è molto meno oneroso rispetto a un unico passaggio drastico e, in ultima analisi, la possibilità di apprendimento in itinere dovrebbe favorire lo sviluppo di processi migliori e scalabili in modo più efficace.
Il passaggio verso un monitoraggio più centralizzato presenta problematiche concrete. Tuttavia, a prescindere dal vostro punto di partenza o da quanto cauta sia la vostra organizzazione nell'affrontare questo concetto, la realtà è che il cambiamento è già in corso ed è meglio rimanere all'avanguardia, anziché farsi superare dalla concorrenza, soprattutto in un settore in cui il time-to-market è tutto.